Abbildung: Nature Methods 9(6), 615–620 (2012). doi:10.1038/nmeth.2014
Das Labor entwickelt fortschrittliche Fluoreszenzbildgebungsverfahren für die präklinische und klinische Anwendung.
Im Jahr 2011 führte dies zur ersten klinischen Übertragung eines zielgerichteten Fluoreszenzmarkers für die optische molekulare Bildgebung beim Menschen. Der Fokus liegt auf der Entwicklung quantitativer, tomographischer und echtzeitfähiger Verfahren, die weit über das konventionelle „fotografische“ Fluoreszenzbild hinausgehen.
Zur Umsetzung dieser Ziele setzen wir multispektrale Techniken sowie theoretische Methoden ein, die die Lichtausbreitung im Gewebe modellieren und eine hochpräzise Bildgebung ermöglichen. Parallel dazu arbeiten wir aktiv an der Validierung von Fluoreszenzmarkern und klinischen Zielstrukturen.
Besondere Forschungsschwerpunkte sind:
Forschungsbereiche

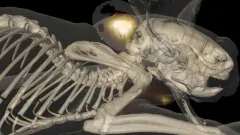
Oben:
Schematische Darstellung des cNIRF-IVUS-Systems.
Unten links:
In-vivo-Bildgebung der Koronararterie mit einem implantierten, NIR-fluoreszierenden, fibrinmarkierten Stent unter Verwendung eines 4,5F/40MHz Hybrid-cNIRF-IVUS-Katheters.
Maßstabsbalken: 1 mm
Unten rechts:
In-vivo-cNIRF-IVUS-Bildgebung von Entzündungen bei Atherosklerose. Repräsentative cNIRF-IVUS-Querschnittsbilder sind in (b) und (c) dargestellt. Vergrößerte Ausschnitte unten links zeigen Hinweise auf Atherosklerose in (b).
Maßstabsbalken: 1 mm
(d) cNIRF-Bild der proteolytischen Aktivität in entzündlichen Plaques.
(e) Korrelierendes ex vivo Fluoreszenzreflexionsbild (FRI) der resezierten Arterie.
Quelle: CBI
- Echtzeitfähige interventionelle fluoreszenzmolekulare Bildgebung
Echtzeitfähige fluoreszenzmolekulare Bildgebung, insbesondere für chirurgische Eingriffe und die chirurgische Endoskopie, mit dem Ziel, Läsionen besser zu identifizieren und Tumorränder präzise abzugrenzen. Die Forschung konzentriert sich auf neuartige multispektrale Bildgebungssysteme sowie auf den Einsatz klinisch relevanter Fluoreszenzmarker (siehe Nat. Med. 2011 17:1315–9 und untenstehende Highlights). - Hybride Fluoreszenzmolekulare Tomographie (FMT) und Röntgen-CT-Bildgebung
Ziel der FMT-Gruppe ist es, das volle Potenzial des hybriden FMT-XCT-Bildgebungssystems auszuschöpfen und neuartige Inversionsverfahren unter Verwendung von Bild-Priors zu entwickeln, um eine präzise, quantitative molekulare In-vivo-Bildgebung bei Kleintieren zu ermöglichen. Darüber hinaus setzen wir FMT-XCT in verschiedenen präklinischen Anwendungen ein, um die Grundlagenforschung und Wirkstoffentwicklung zu unterstützen. - Fluoreszenz- und Farbkryoschnittbildgebung
Fluoreszenz- und Farbkryoschnittverfahren zur genauen Bestimmung der Biodistribution von Fluoreszenzmarkern, markierten Zellen und Gewebezuständen. Parallel dazu entwickeln wir multispektrale Bildgebungsverfahren zur automatisierten Gewebeabbildung während des Kryoschnitts. Aktuelle Forschungsschwerpunkte liegen in der Optimierung der Hardware sowie in der Entwicklung von Bildgebungsverfahren zur Korrektur von Lichtstreuung, um eine überlegene Quantifizierung im Vergleich zu einfachen fotografischen Fluoreszenzbildern zu erreichen. - Standardisierung und Benchmarking von Fluoreszenzbildgebungssystemen
Wir erforschen die Entwicklung von Algorithmen und Phantomen zur Standardisierung von Fluoreszenzkameras. Dies umfasst die Validierung von Leistungskennzahlen, die Korrektur von Beleuchtungsartefakten sowie die Entwicklung von Benchmark-Tests, die langfristig eine hochpräzise fluoreszenzmolekulare Bildgebung ermöglichen sollen. - Intravasculäre NIRF Bildgebung
Wir integrieren die Entwicklung eines cNIRF-IVUS-Katheters (c = korrigiert), der eine simultane, ko-registrierte Bildgebung durch Blut hindurch ermöglicht, um krankheitsbedingte morphologische und biologische Veränderungen in den Koronar- und peripheren Arterien in vivo darzustellen. Wir haben hybride Katheter mit 9F/15 MHz für periphere Gefäße und 4,5F/40 MHz für Koronararterien entwickelt und in Schweine- und Kaninchenmodellen getestet. Ein Korrekturalgorithmus, der auf IVUS-Informationen basiert, wurde entwickelt, um die durch blutbedingte, distanzabhängige Abschwächung des Fluoreszenzsignals zu kompensieren.
Forschungs-Highlights
Klinische Übertragung der fluoreszenzmolekularen Bildgebung
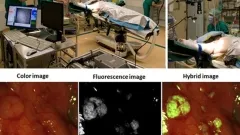
Oben: Klinisches IBMI-System, installiert für Brustkrebsoperationen am Universitätsklinikum Groningen, Niederlande.
Unten: Echtzeit-Visualisierung einer Operation bei Eierstockkrebs an einer Patientin, die mit einer fluoreszierenden, folatrezeptor-spezifischen Sonde behandelt wurde (Bild aus van Dam G. et al., Nature Medicine, 2011).
Quelle: Phil. Trans. R. Soc. A 369(1955), 4666–4678 (2011). doi:10.1098/rsta.2011.0270 (oben rechts) Nature Medicine 17(10): 1315–1319 (2011). doi:10.1038/nm.2472 (unten)
Klinische Übertragung der fluoreszenzmolekularen Bildgebung
Unsere Gruppe überträgt neuartige molekulare Bildgebungsverfahren in die klinische interventionelle Bildgebung, mit dem Ziel, das Paradigma der Krankheitsdetektion bei chirurgischen und endoskopischen Eingriffen grundlegend zu verändern. Die in Abbildung 3 gezeigte Arbeit zeigt unsere Fluoreszenzkamera im Operationssaal (in Zusammenarbeit mit Prof. Van Dam, UMCG) sowie Ergebnisse einer Patientin mit Eierstockkrebs. Die Ergebnisse demonstrieren die Integration neuartiger Bildgebungsverfahren mit der klinischen Anwendung eines fluoreszierenden Wirkstoffs, der gezielt den Folatrezeptor Alpha adressiert – ein Rezeptor, der bei Eierstockkrebs verstärkt exprimiert wird. Diese Studie (Nat. Med. 2011; 17:1315–1319) zeigte die erste Anwendung eines gezielten fluoreszierenden Farbstoffs beim Menschen. Die Bildgebung erfolgt über ein Kamerasystem, das Farbe und Nahinfrarot-Fluoreszenz (NIR) in Echtzeit erfassen und auflösen kann. In den kommenden Jahren wird die klinische Übertragung weiterer Wirkstoffe erwartet, um eine größere Bandbreite an Erkrankungen abzudecken.
In Science Translational Medicine haben wir zudem die Herausforderungen bei der klinischen Übertragung fluoreszierender Wirkstoffe beschrieben und einen Überblick über alternative Strategien gegeben, um diesen Herausforderungen zu begegnen und das Risiko sowie den Investitionsaufwand für den interventionellen Einsatz zu minimieren. Weitere Details finden sich in Scheuer et al., Sci. Transl. Med. 2012; 4:134ps11.
Multispektrale Fluoreszenzbildgebung und Endoskopie
Bei vielen interventionellen Verfahren, wie chirurgischen Eingriffen oder diagnostischer bzw. chirurgischer Endoskopie, basiert die klinische Entscheidungsfindung noch immer auf dem visuellen Erscheinungsbild oder dem Abtasten von Läsionen und Gewebearealen.
Die Chirurgie steht dabei vor Herausforderungen bei der Identifikation von Tumorausbreitungen und der genauen Abgrenzung von Tumorrändern, was zu unvollständigen Tumorresektionen führen kann und die Prognose der Patient:innen gefährdet.
Auch die Überwachung und endoskopische Entfernung von Läsionen leidet unter dem geringen Kontrast zwischen kleinen malignen Läsionen und benignem Gewebe sowie dem Mangel an Informationen über die Tiefe der Läsionen, was die Detektion und die Wahl des geeigneten Eingriffs erschwert. Die multispektrale Fluoreszenzbildgebung und Endoskopie entwickeln sich als vielversprechende Ansätze zur interventionellen Unterstützung. Eine erhöhte Detektionssensitivität und -spezifität kann durch die Kombination von großflächiger Fluoreszenzbildgebung mit gezielten Wirkstoffen erreicht werden, wodurch bislang unsichtbare Krankheitsmarker erkannt werden können.
Aus diesem Grund konzentriert sich die aktuelle Forschung auf die gleichzeitige Erfassung von Farbe und NIR-Fluoreszenz in flexiblen Endoskopen und Laparoskopen, die routinemäßig in der klinischen Überwachungsendoskopie und Therapiekontrolle eingesetzt werden.
Ein Mehrkanal-Kamerasystem wurde für die intraoperative und endoskopische Fluoreszenzbildgebung entwickelt. Die gleichzeitige Aufnahme von Farb- und NIR-Fluoreszenzbildern wird durch einen dichroitischen Spiegel und eine speziell entwickelte Software ermöglicht. Die Verarbeitung der Daten in Video-Rate erfolgt durch GPU-basiertes Computing. Das System lässt sich problemlos in Operationssäle sowie chirurgische und Überwachungsverfahren integrieren und wurde bereits in mehreren klinischen Studien eingesetzt.
Die Bildverwaltung und -analyse basiert auf theoretischen Modellen der Photon-Gewebe-Interaktion, um eine präzise, echte quantitative Fluoreszenzbildgebung zu ermöglichen – also eine Bildgebung, die unabhängig von den optischen Eigenschaften des Gewebes ist – sowie eine Normalisierung hinsichtlich der Beleuchtung und Detektion des Systems. Dies führt zu einer Minimierung von Fehlalarmen und falsch-negativen Ergebnissen. Die Kombination dieser Aufnahme- und Analyseverfahren bietet eine neue Generation der Fluoreszenzbildgebung für die Klinik, um die chirurgische und endoskopische Sicht zu verbessern.
FMT-XCT
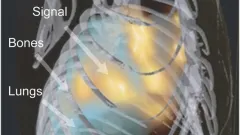
Basierend auf XCT-Daten und FMT-Rekonstruktion einer K-ras-Maus mit Lungentumoren.
Quelle: Nature Methods 9(6), 615–620 (2012). doi:10.1038/nmeth.2014
Die Entwicklungen in der Fluoreszenzbildgebung haben auch zur Entstehung hybrider Verfahren wie der Fluoreszenz-Molekular-Tomographie (FMT) in Kombination mit der Röntgen-Computertomographie (XCT) geführt (siehe Ale et al., Nature Methods 2012, 9(6), 615–620).
Diese Ansätze verändern grundlegend die Möglichkeiten, zelluläre und subzelluläre Prozesse bei Tieren und Menschen zu erkennen, indem sie eine Art „in vivo-Färbung“ wichtiger Biomoleküle ermöglichen, die eine entscheidende Rolle bei Krankheitsverläufen oder Therapien spielen. Dadurch eröffnen sich neue Wege für explorative, diagnostische und theranostische Verfahren.
Maßgebliche Publikationen
Bozhko D, Osborn EA, Rosenthal A, Verjans JWH, Hara T, McCarthy JR, Kellnberger S, Wissmeyer G, Ovespian SV, Mauskapf A, Stein AF, Jaffer FA, Ntziachristos V. Quantitative Intravascular Biological Fluorescence-Ultrasound Imaging of Coronary and Peripheral Arteries In Vivo. EHJCI, in press.
Teresa C., Maximilian K., Angelique A., Vasilis N., and Simon A. Patch-based anisotropic diffusion scheme for fluorescence diffuse optical tomography-part 2: Image reconstruction, Phys Med Biol 61(4), 1452-1475 (2016).
Koch M., and Ntziachristos V. Advancing surgical vision with fluorescence imaging, Annu Rev Med 67(1), 153-164 (2016).
Tjalma J. J., Garcia-Allende P. B., Hartmans E., Terwisscha van Scheltinga A. G., Boersma-van Ek W., Glatz J., Koch M., van Herwaarden Y. J., Bisseling T. M., Nagtegaal I. D., Timmer-Bosscha H., Koornstra J. J., Karrenbeld A., Kleibeuker J. H., van Dam G. M., Ntziachristos V., and Nagengast W. B. Molecular fluorescence endoscopy targeting vascular endothelial growth factor a for improved colorectal polyp detection, J Nucl Med 57(3), 480-485 (2016).
Mohajerani P., Koch M., Thürmel K., Haller B., Rummeny E. J., Ntziachristos V., and Meier R. Fluorescence-aided tomographic imaging of synovitis in the human finger, Radiology 272(3), 865-874 (2014).
Koch M., Glatz J., Ermolayev V., de Vries E. G. E., van Dam G. M., Englmeier K.-H., and Ntziachristos V. Video-rate optical flow corrected intraoperative functional fluorescence imaging, J Biomed Opt 19(4), 046012-046012 (2014).
Garcia-Allende P. B., Glatz J., Koch M., Tjalma J. J., Hartmans E., Terwisscha van Scheltinga A. G. T., Symvoulidis P., van Dam G. M., Nagengast W. B., and Ntziachristos V. Towards clinically translatable NIR fluorescence molecular guidance for colonoscopy, Biomed Opt Express 5(1), 78-92 (2014).
Glatz J., Garcia-Allende P. B., Becker V., Koch M., Meining A., and Ntziachristos V. Near-infrared fluorescence cholangiopancreatoscopy: Initial clinical feasibility results, Gastrointest Endosc 79(4), 664-668 (2014).
Glatz J., Varga J., Garcia-Allende P. B., Koch M., Greten F. R., and Ntziachristos V. Concurrent video-rate color and near-infrared fluorescence laparoscopy, J Biomed Opt 18(10), 101302-101302 (2013).
Correia T., Rudge T., Koch M., Ntziachristos V., and Arridge S. Wavelet-based data and solution compression for efficient image reconstruction in fluorescence diffuse optical tomography, J Biomed Opt 18(8), 086008-086008 (2013).
Garcia-Allende P. B., Glatz J., Koch M., and Ntziachristos V. Enriching the interventional vision of cancer with fluorescence and optoacoustic imaging, J Nucl Med 54(5), 664-667 (2013).
Ale A., Ermolayev V., Herzog E., Cohrs C., de Angelis M. H., and Ntziachristos V. FMT-XCT: In vivo animal studies with hybrid fluorescence molecular tomography-x-ray computed tomography, Nat Methods 9(6), 615-620 (2012).
Mallas G, Brooks DH, Rosenthal A, Nudelman RN, Mauskapf A, Jaffer FA, Ntziachristos V. Improving quantification of intravascular fluorescence imaging using structural information. Phys Med Biol 57(20), 6395-6406 (2012).
Scheuer W., van Dam G. M., Dobosz M., Schwaiger M., and Ntziachristos V. Drug-based optical agents: Infiltrating clinics at lower risk, Sci Transl Med 4(134), 134ps11-134ps11 (2012).
van Dam G. M., Themelis G., Crane L. M. A., Harlaar N. J., Pleijhuis R. G., Kelder W., Sarantopoulos A., de Jong J. S., Arts H. J. G., van der Zee A. G. J., Bart J., Low P. S., and Ntziachristos V. Intraoperative tumor-specific fluorescence imaging in ovarian cancer by folate receptor-[alpha] targeting: First in-human results, Nat Med 17(10), 1315-1319 (2011).
Jaffer FA, Calfon MA, Rosenthal A, Mallas G, Razansky RN, Mauskapf A, Weissleder R, Libby P, Ntziachristos V. Two-dimensional intravascular near-infrared fluorescence molecular imaging of inflammation in atherosclerosis and stent-induced vascular injury. J Am Coll Cardiol 57(25), 2516-2526 (2011).
Crane L. M. A., Themelis G., Pleijhuis R. G., Harlaar N. J., Sarantopoulos A., Arts H. J. G., van der Zee A. G. J., Vasilis N., and van Dam G. M. Intraoperative multispectral fluorescence imaging for the detection of the sentinel lymph node in cervical cancer: A novel concept, Mol Imaging Biol 13(5), 1043-1049 (2011).